Una reacción de descomposición es un tipo de reacción química en la que un compuesto (reactivo) se descompone en dos o más productos, que son más simples que el reactivo del que proceden.
Su ecuación general es la siguiente:
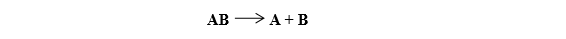
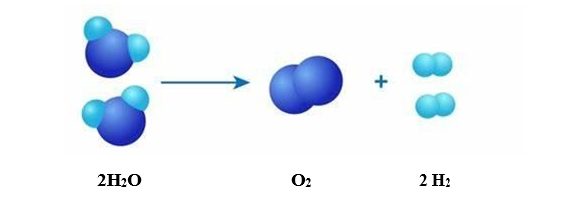
Un ejemplo sería la electrólisis del agua (H2O):
👉Consulta nuestros niveles:
Es uno de los cuatro tipos principales de reacciones químicas, su reacción opuesta es una reacción de síntesis, dónde reaccionan dos o más reactivos y forman un producto más complejo.
Cuándo ocurre una reacción de descomposición
Las reacciones de descomposición suelen ocurrir cuando se aplica calor, luz o electricidad.
Tipos de reacciones de descomposición
Dentro de las reacciones de descomposición existen varios tipos:
- Descomposición térmica: Ocurre la descomposición cuando se aplica calor. Un ejemplo es la descomposición del carbonato cálcico (CaCO3) para formar óxido de calcio y dióxido de carbono.
- Descomposición electrolítica: Ocurre al suministrar energía eléctrica. Un ejemplo es la electrólisis del agua.
- Fotólisis: Ocurre cuando el reactivo absorbe luz (fotones) para romper los enlaces y formar los productos. Un ejemplo es la descomposición del peróxido de hidrógeno (H2O2).
Cómo pueden ser las reacciones de descomposición
Las reacciones de descomposición suelen ser endotérmicas y necesitan más energía de la que liberan, aunque hay ciertas excepciones en las que esto sucede al contrario y requieren menos energía de la que liberan en el proceso, siendo por tanto exotérmicas, como es el caso de la descomposición del óxido nitroso:
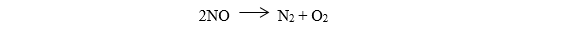
👉Consulta nuestras academias:





Deja una respuesta